Assimilat Allokation und NMR
Pflanzen besitzen ein feines Adergeflecht - die Vaskulatur - um Nährstoffe zu verteilen, doch was kontrolliert die entsprechenden Transportprozesse? Wie gelangen Zucker und Aminosäuren in den Samen? Wie werden hieraus Speicherstoffe synthetisiert? Können wir den Nährstoffimport und die Syntheseleistung von Samen und anderen Speicherorganen erhöhen, um letztlich den Ertrag von Kulturpflanzen zu steigern? Wir suchen nach Antworten auf diese und weitere Fragen.
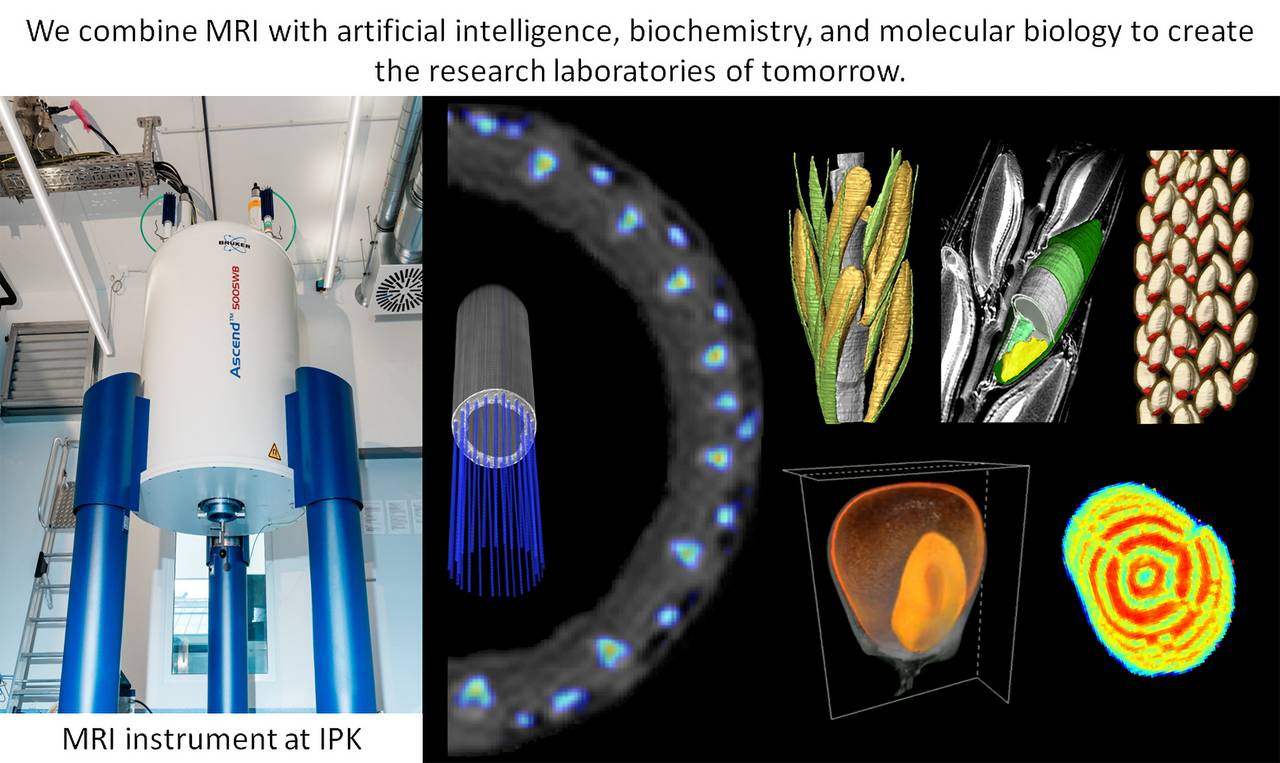
Unsere Forschung basiert auf Magnetresonanz-Imaging (MRI) - einem zerstörungsfreien, bildgebenden Verfahren, bekannt aus medizinischer Forschung und Diagnostik. Wir entwickeln MRI für Pflanzen, zur Analyse von Transportprozessen, Wachstum und Ertragsbildung bei Kulturpflanzen.
Neue Entwicklungen in der MRI erweitern das Spektrum des Möglichen, indem sie unser Verständnis vom Innenleben der Pflanzen revolutionieren und neue Möglichkeiten in der Pflanzenzüchtung und Biotechnologie eröffnen. Wir nutzen die Stärken unserer strategischen Partnerschaften mit führenden NMR-Physikern und Biologen auf der ganzen Welt. Unser interdisziplinäres Team kombiniert MRI mit künstlicher Intelligenz, Biochemie und Molekularbiologie, um die Forschungslabore von morgen zu schaffen.
scroll top
Projekte
Aktuelle Forschungsthemen
Unser Forschungsansatz, unsere Methoden und Werkzeuge erlauben Zugang zu einer Vielzahl relevanter Forschungsthemen. In aktuellen Projekten bearbeiten wir anhand wichtiger Kulturpflanzen wie Gerste, Mais, Raps, Leguminosen und Wasserlinsen folgende Fragestellungen.
Assimilatversorgung und Samenfüllung: Untersuchungen zur Zucker- und Aminosäureaufnahme von Samen basierend auf der Charakterisierung spezifischer Gene/Proteine, der Visualisierung von Transportprozessen und Vaskulatur.
Pflanzliche Entwicklungsprozesse: in vivo Analyse von Embryonalentwicklung, Blütenentwicklung und Samenkeimung.
Hypoxie in Samen: Untersuchungen zur spezifischen Anpassung von Samen an niedrige, endogene Sauerstoffkonzentrationen, wie sie typischerweise während der Samenentwicklung auftreten.
Speicherstoffsynthesen und deren Regulation: Charakterisierung von Genen/Proteinen, welche die Umwandlung von Assimilaten in Speicherstoffe (Öl, Protein, Stärke) und deren Akkumulation steuern.
MAGDI: Schaffung neuer Verfahren der Phänotypisierung und Arbeitswerkzeuge für die Pflanzenzucht durch Verknüpfung von MRI mit künstlicher Intelligenz. Link: https://www.dip-sachsen-anhalt.de/projekt/dip-magdi/
Pflanze/Mikrobiom-Interaktionen: Analyse der Interaktionen zwischen Mikroorganismen und den am schnellsten wachsenden Kulturpflanzen unseres Planeten (Wasserlinsen).
Programmierter Zelltod (PCD): Untersuchungen zur Steuerung von PCD in Samen und seiner Rolle für Nährstoffaufnahme und Samenfüllung.
Karriere
Wir suchen Menschen, die bereit sind, sich mit Herz und Energie der Pflanzenforschung zu widmen. Wir fördern ein Umfeld, in dem die Erfahrungen und Fachkenntnisse jedes Einzelnen geschätzt werden. Wir sind neugierig und beharrlich in unseren Bemühungen, langfristige, nachhaltige Innovationen voranzutreiben, um die größten Herausforderungen der Menschheit zu bewältigen.
Und wir möchten allen ehemaligen Mitarbeitern des Teams unseren herzlichen Dank aussprechen, deren enthusiastisches Engagement diese Forschungsarbeit ermöglicht hat.
scroll top
Mitarbeitende
scroll top
Publikationen
Borisjuk L, Neuberger T, Rolletschek H:
Lipid MRI in plant science: principles and potential areas of application. J. Exp. Bot. (2026) accepted. https://dx.doi.org/10.1093/jxb/eraf479
Isayenkov S, Borisjuk L, Mayer S, Hilo A, Knoch D, Meitzel T, Hause B, Tandron Moya Y A, Rolletschek H, Peiter E, Radchuk V:
Root structural and metabolic plasticity confers tolerance to salinity in wild barley species grown under waterlogging. Plant Cell Environ. (2026) Epub ahead of print. https://dx.doi.org/10.1111/pce.70563
Lee Y, Braglia L, Stepanenko A, Fuchs J, Schubert V, Gianì S, Romano L E, Aronne G, Forti C, Schubert I, Morello L:
Hybridity of mainly asexually propagating duckweeds in genus Lemna - dead end or breakthrough? New Phytol. 250 (2026) 629-647. https://dx.doi.org/10.1111/nph.70748
Lee Y, Schubert V, Stepanenko A, Kim G, Braglia L, Schubert I, Morello L:
Newly unveiled meiosis elucidates the unreduced gamete frequency and its impact on the evolution of the Lemna minor complex. J. Exp. Bot. (2026) accepted. https://dx.doi.org/10.1093/jxb/erag215
Milyaev A, Frolov A, Lempe J, Hilo A, Luedeling E, Wessjohann L A, Flachowsky H, Wünsche J-N:
Carbohydrate analyses indicate that fruit-bud competition for assimilates is not the primary trigger of biennial bearing in apple. J. Plant Physiol. 316 (2026) 154666. https://dx.doi.org/10.1016/j.jplph.2025.154666
Rolletschek H, Borisjuk L:
When solids become fluid to sustain life. New Phytol. (2026) Epub ahead of print. https://dx.doi.org/10.1111/nph.71299
Shi H, McGinn M, Hing N Y K, Jarvis B A, Gautam B, Kuczynski C, Hilo A, Rolletschek H, Sedbrook J C, Schwender J:
Metabolic flux, metabolite, and transcript analysis uncover reprogramming of metabolism toward higher seed oil. Plant Physiol. 201 (2026) kiag148. https://dx.doi.org/10.1093/plphys/kiag148
Stepanenko A, Schubert V, Chen G, Kishchenko O, Michael T P, Lam E, Hrmova M, Schubert I, Borisjuk N:
Genome sequence assembly of the 5S rDNA loci informs haplotype specificity and evolution in the greater duckweed Spirodela polyrhiza. Commun. Biol. 9 (2026) 516. https://dx.doi.org/10.1038/s42003-026-09598-8
Borisjuk L, Neuberger T:
Perspectives: The look insight - magnetic resonance imaging (MRI) of the inner life of plants. J. Plant Physiol. 309 (2025) 154502. https://dx.doi.org/10.1016/j.jplph.2025.154502
Knoch D, Rugen N, Thiel J, Heuermann M C, Kuhlmann M, Rizzo P, Meyer R C, Wagner S, Schippers J H M, Braun H-P, Altmann T:
A spatio-temporal transcriptomic and proteomic dataset of developing Brassica napus seeds. Sci. Data 12 (2025) 759. https://dx.doi.org/10.1038/s41597-025-05115-4
Langkutsch C:
Selektion homozygoter Linien von umamit-Mutanten und deren phänotypische Charakterisierung. (Bachelor Thesis) Köthen, Hochschule Anhalt, Fachbereich Angewandte Biowissenschaften und Prozesstechnik (2025) 40 pp.
Plutenko I, Radchuk V, Mayer S, Keil P, Ortleb S, Wagner S, Lehmann V, Rolletschek H, Borisjuk L:
MRI-Seed-Wizard: combining deep learning algorithms with magnetic resonance imaging enables advanced seed phenotyping. J. Exp. Bot. 76 (2025) 393-410. https://dx.doi.org/10.1093/jxb/erae408
Rolletschek H, Borisjuk L, Gómez-Álvrez E M, Pucciariello C:
Advances in seed hypoxia research - an updated review. Plant Physiol. 197 (2025) kiae556. https://dx.doi.org/10.1093/plphys/kiae556
Sahu A, Psaroudakis D, Rolletschek H, Neumann K, Borisjuk L, Himmelbach A, Pinninti K, Knoch D, Töpfer N, Szymanski J:
panomiX: Investigating mechanisms of trait emergence through multi-omics data integration. Plant Phenomics 7 (2025) 100131. https://doi.org/10.1016/j.plaphe.2025.100131
Schüler D, Lange M, Altmann T, Cuacos M, Arend D, D’Auria J C, Fiebig A, Kumlehn J, Neumann K, Melzer M, Rey-Mazón E, Rolletschek H, Scholz U, Willner E, Reif J C:
Data management in balance – a decade of balancing pragmatism, sustainability and innovation at plant research center IPK Gatersleben. J. Integr. Bioinform. 22 (2025) 20250012. https://dx.doi.org/10.1515/jib-2025-0012
Hinrichs P:
Comparative study of maize kernels with magnetic resonance imaging and semantic segmentation. (Master Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2024) 84 pp.
Langer M:
Investigations on maize kernel development and the relevance of endogenous hypoxia. (PhD Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2024) 124 pp.
Mayer S, Rolletschek H, Radchuk V, Wagner S, Ortleb S, Gündel A, Dehmer K J, Gutjahr F T, Jakob P M, Borisjuk L:
Metabolic imaging in living plants: A promising field for chemical exchange saturation transfer (CEST) MRI. Sci. Adv. 10 (2024) eadq4424. https://dx.doi.org/10.1126/sciadv.adq4424
Meitzel T:
Good things come to those who wait - a 42-yr study challenges 'trade-off' theories. New Phytol. 241 (2024) 521-522. https://dx.doi.org/10.1111/nph.19350
Rezaeva B R, Rutten T, Bollmann C, Ortleb S, Melzer M, Kumlehn J:
Plant regeneration via adventitious shoot formation from immature zygotic embryo explants of Camelina. Plants 13 (2024) 465. https://dx.doi.org/10.3390/plants13040465
Rolletschek H, Muszynska A, Schwender J, Radchuk V, Heinemann B, Hilo A, Plutenko I, Keil P, Ortleb S, Wagner S, Kalms L, Gündel A, Shi H, Fuchs J, Szymanski J J, Braun H-P, Borisjuk L:
Mechanical forces orchestrate the metabolism of the developing oilseed rape embryo. New Phytol. 244 (2024) 1328-1344. https://dx.doi.org/10.1111/nph.19990
Rutten T, Thirulogachandar V, Huang Y, Shanmugaraj N, Koppolu R, Ortleb S, Hensel G, Kumlehn J, Melzer M, Schnurbusch T:
Anatomical insights into the vascular lay-out of the barley rachis: implications for transport and spikelet connection. Ann. Bot. 133 (2024) 983-996. https://dx.doi.org/10.1093/aob/mcae025
Vogelsang N:
Complementation of the yeast Δtps2 deletion mutant by expression of TPPs involved in wheat floret abortion. (Master Thesis) Köthen, Hochschule Anhalt, Fachbereich Angewandte Biowissenschaften und Prozesstechnik (2024)
Wamhoff D, Gündel A, Wagner S, Ortleb S, Borisjuk L, Winkelmann T:
Anatomical limitations in adventitious root formation revealed by magnetic resonance imaging, infrared spectroscopy, and histology of rose genotypes with contrasting rooting phenotypes. J. Exp. Bot. 75 (2024) 4784-4801. https://dx.doi.org/10.1093/jxb/erae158
Yu P, Li C, Li M, He X, Wang D, Li H, Marcon C, Li Y, Perez-Limón S, Chen X, Delgado-Baquerizo M, Koller R, Metzner R, van Dusschoten D, Pflugfelder D, Borisjuk L, Plutenko I, Mahon A, Resende M F R J, Salvi S, Akale A, Abdalla M, Ahmed M A, Bauer F M, Schnepf A, Lobet G, Heymans A, Suresh K, Schreiber L, McLaughlin C M, Li C, Mayer M, Schön C-C, Bernau V, von Wirén N, Sawers R J H, Wang T, Hochholdinger F:
Seedling root system adaptation to water availability during maize domestication and global expansion. Nat. Genet. 56 (2024) 1245-1256. https://dx.doi.org/10.1038/s41588-024-01761-3
Alomari D Z, Schierenbeck M, Alqudah A M, Alqahtani M D, Wagner S, Rolletschek H, Borisjuk L, Röder M S:
Wheat grains as a sustainable source of protein for health. Nutrients 15 (2023) 4398. https://dx.doi.org/10.3390/nu15204398
Bellin L, Melzer M, Hilo A, Amaya D L G, Keller I, Meurer J, Möhlmann T:
Nucleotide limitation results in impaired photosynthesis, reduced growth and seed yield together with massively altered gene expression. Plant Cell Physiol. 64 (2023) 1494-1510. https://dx.doi.org/10.1093/pcp/pcad063
Borisjuk L, Horn P, Chapman K, Jakob P M, Gündel A, Rolletschek H:
Seeing plants as never before. New Phytol. 238 (2023) 1775-1794. https://dx.doi.org/10.1111/nph.18871
Gündel A:
Multimodal imaging unveils the hidden dimensions of plant physiology: from metabolic landscapes to mechanistic insights. (PhD Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2023) 240 pp.
Keil P, Gündel B, Gündel A, Rolletschek H, Borisjuk L:
Non-invasive single-grain screening of proteins and other features by combination of near-infrared spectroscopy and nuclear magnetic resonance. Agronomy 13 (2023) 1393. https://dx.doi.org/10.3390/agronomy13051393
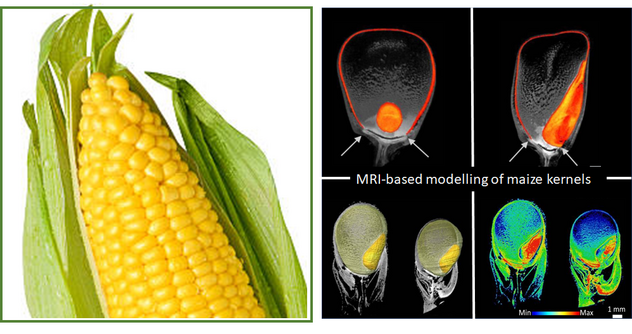
Langer M, Hilo A, Guan J-C, Koch K E, Xiao H, Verboven P, Gündel A, Wagner S, Ortleb S, Radchuk V, Mayer S, Nicolai B, Borisjuk L, Rolletschek H:
Causes and consequences of endogenous hypoxia on growth and metabolism of developing maize kernels. Plant Physiol. 192 (2023) 1268-1288. https://dx.doi.org/10.1093/plphys/kiad038
Mira M M, Hill R D, Hilo A, Langer M, Robertson S, Igamberdiev A U, Wilkins O, Rolletschek H, Stasolla C:
Plant stem cells under low oxygen: metabolic rewiring by phytoglobin underlies stem cell functionality. Plant Physiol. 193 (2023) 1416-1432. https://dx.doi.org/10.1093/plphys/kiad344
Plutenko I, Papkov M, Palo K, Parts L, Fishman D:
Metadata improves segmentation through multitasking elicitation. In: Koch L, Cardoso M J, Ferrante E, Kamnitsas K, Islam M, Jiang M, Rieke N, Tsaftaris S A, Yang D (Eds.): Domain adaptation and representation transfer. DART 2023. (Series: Lecture Notes in Computer Science, Vol. 14293) Cham: Springer (2023) ISBN 978-3-319-23107-5, 147-155. https://dx.doi.org/10.1007/978-3-031-45857-6_15
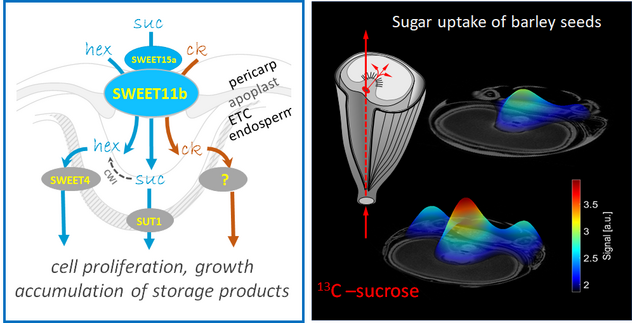
Radchuk V, Belew Z M, Gündel A, Mayer S, Hilo A, Hensel G, Sharma R, Neumann K, Ortleb S, Wagner S, Muszynska A, Crocoll C, Xu D, Hoffie I, Kumlehn J, Fuchs J, Peleke F F, Szymanski J J, Rolletschek H, Nour-Eldin H H, Borisjuk L:
SWEET11b transports both sugar and cytokinin in developing barley grains. Plant Cell 35 (2023) 2186-2207. https://dx.doi.org/10.1093/plcell/koad055
Shi H, Ernst E, Heinzel N, McCorkle S, Rolletschek H, Borisjuk L, Ortleb S, Martienssen R, Shanklin J, Schwender J:
Mechanisms of metabolic adaptation in the duckweed Lemna gibba: an integrated metabolic, transcriptomic and flux analysis. BMC Plant Biol. 23 (2023) 458. https://dx.doi.org/10.1186/s12870-023-04480-9
Teh J T, Leitz V, Holzer V J C, Neusius D, Marino G, Meitzel T, García-Cerdán J G, Dent R M, Niyogi K K, Geigenberger P, Nickelsen J:
NTRC regulates CP12 to activate Calvin-Benson cycle during cold acclimation. Proc. Natl. Acad. Sci. U.S.A. 120 (2023) e2306338120. https://dx.doi.org/10.1073/pnas.2306338120
Blume R Y, Yemets A I, Korkhovyi V, Radchuk V, Rakhmetov D, Blume Y B:
Genome-wide identification and analysis of cytokinin oxidase/dehydrogenase (ckx) gene family in finger millet (Eleusine coracana) Front. Genet. 13 (2022) 963789. https://dx.doi.org/10.3389/fgene.2022.963789
Bouquet F:
Mechanismen der molekularen und biochemischen Anpassung zu Hypoxie in Maissamen. (Master Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät, Institut für Pflanzengenetik (2022) 86 pp.
Mayer S, Munz E, Hammer S, Wagner S, Guendel A, Rolletschek H, Jakob P M, Borisjuk L, Neuberger T:
Quantitative monitoring of paramagnetic contrast agents and their allocation in plant tissues via DCE-MRI. Plant Methods 18 (2022) 47. https://dx.doi.org/10.1186/s13007-022-00877-z
Nagel M, Arc E, Rajjou L, Cueff G, Bailly M, Clément G, Sanchez-Vicente I, Bailly C, Seal C E, Roach T, Rolletschek H, Lorenzo O, Börner A, Kranner I:
Impacts of drought and elevated temperature on the seeds of malting barley. Front. Plant Sci. 13 (2022) 1049323. https://dx.doi.org/10.3389/fpls.2022.1049323
Plaehn N M J, Mayer S, Jakob P M, Gutjahr F T:
T1-independent exchange rate quantification using saturation- or phase sensitive-water exchange spectroscopy. J. Magn. Reson. 335 (2022) 107141. https://dx.doi.org/10.1016/j.jmr.2021.107141
Schüler V J:
Analyse des Interaktionsmechanismus des Nuclear Factor Y Komplexes in Gerstenkörnern. (Bachelor Thesis) Köthen, Hochschule Anhalt, Fachbereich Angewandte Biowissenschaften und Prozesstechnik (2022) 61 pp.
Acosta K, Appenroth K J, Borisjuk L, Edelman M, Heinig U, Jansen M A K, Oyama T, Pasaribu B, Schubert I, Sorrels S, Sree K S, Xu S, Michael T P, Lam E:
Return of the Lemnaceae: Duckweed as a model plant system in the genomics and post-genomics era. Plant Cell 33 (2021) 3207-3234. https://dx.doi.org/10.1093/plcell/koab189
Fiebelkow J, Guendel A, Guendel B, Mehwald N, Jetka T, Komorowski M, Waldherr S, Schaper F, Dittrich A:
The tyrosine phosphatase SHP2 increases robustness and information transfer within IL-6-induced JAK/STAT signalling. Cell Commun. Signal. 19 (2021) 94. https://dx.doi.org/10.1186/s12964-021-00770-7
Goelckel L:
Cellular plasticity and mechanosensing in the Brassica napus embryo. (Master Thesis) Halle/S., Martin-Luther-Universität Halle-Wittenberg, Naturwissenschaftliche Fakultät I Biowissenschaften, Institut für Biologie (2021) 61 pp.
Gomez-Sanchez A, Santamaria M E, Gonzalez-Melendi P, Muszynska A, Matthess C, Martinez M, Diaz I:
Repression of barley cathepsins, HvPap-19 and HvPap-1, differentially alters grain composition and delays germination. J. Exp. Bot. 72 (2021) 3474-3485. https://dx.doi.org/10.1093/jxb/erab007
Guendel A, Hilo A, Rolletschek H, Borisjuk L:
Probing the metabolic landscape of plant vascular bundles by infrared fingerprint analysis, imaging and mass spectrometry. Biomolecules 11 (2021) 1717. https://dx.doi.org/10.3390/biom11111717
Meitzel T, Radchuk R, McAdam E L, Thormählen I, Feil R, Munz E, Hilo A, Geigenberger P, Ross J J, Lunn J E, Borisjuk L:
Trehalose 6-phosphate promotes seed filling by activating auxin biosynthesis. New Phytol. 229 (2021) 1553-1565. https://dx.doi.org/10.1111/nph.16956
Michael T P, Ernst E, Hartwick N, Chu P, Bryant D, Gilbert S, Ortleb S, Baggs E L, Sree K S, Appenroth K J, Fuchs J, Jupe F, Sandoval J P, Krasileva K V, Borisjuk L, Mockler T C, Ecker J, Martienssen R A, Lam E:
Genome and time-of-day transcriptome of Wolffia australiana link morphological minimization with gene loss and less growth control. Genome Res. 31 (2021) 225-238. https://dx.doi.org/10.1101/gr.266429.120
Muszynska A, Guendel A, Melzer M, Tandrón Moya Y, Röder M, Rolletschek H, Rutten T, Munz E, Melz G, Ortleb S, Borisjuk L, Börner A:
A mechanistic view on lodging resistance in rye and wheat: a multiscale comparative study. Plant Biotechnol. J. 19 (2021) 2646-2661. https://dx.doi.org/10.1111/pbi.13689
Radchuk V, Tran V, Hilo A, Muszynska A, Gündel A, Wagner S, Fuchs J, Hensel G, Ortleb S, Munz E, Rolletschek H, Borisjuk L:
Grain filling in barley relies on developmentally controlled programmed cell death. Commun. Biol. 4 (2021) 428. https://dx.doi.org/10.1038/s42003-021-01953-1
Rolletschek H:
Hardy Rolletschek. New Phytol. 232 (2021) 476-478. https://dx.doi.org/10.1111/nph.17567
Rolletschek H, Mayer S, Boughton B, Wagner S, Ortleb S, Kiel C, Roessner U, Borisjuk L:
The metabolic environment of the developing embryo: A multidisciplinary approach on oilseed rapeseed. J. Plant Physiol. 265 (2021) 153505. https://dx.doi.org/10.1016/j.jplph.2021.153505
Rolletschek H, Muszynska A, Borisjuk L:
The process of seed maturation is influenced by mechanical constraints. New Phytol. 229 (2021) 19-23. https://dx.doi.org/10.1111/nph.16815
Vogelsang N:
A novel sensor to map the trehalose 6-phosphate distribution in planta. (Bachelor Thesis) Köthen, Hochschule Anhal (2021) 43 pp.
Borisjuk L, Rolletschek H, Radchuk V:
Advances in understanding of barley plant physiology: factors determining grain development and composition/chemistry. In: Fox G, Li C (Eds.): Achieving sustainable cultivation of barley. (Burleigh Dodds Series in Agricultural Science, Vol. 74) Cambridge, UK: Burleigh Dodds (2020) ISBN 978-1-78676-308-2, 53-96. https://dx.doi.org/10.19103/AS.2019.0060.03
Impe D, Reitz J, Köpnick C, Rolletschek H, Börner A, Senula A, Nagel M:
Assessment of pollen viability for wheat. Front. Plant Sci. 10 (2020) 1588. https://dx.doi.org/10.3389/fpls.2019.01588
Isayenkov S, Hilo A, Rizzo P, Tandron Moya Y A, Rolletschek H, Borisjuk L, Radchuk V:
Adaptation strategies of halophytic barley Hordeum marinum spp marinum to high salinity and osmotic stress. Int. J. Mol. Sci. 21 (2020) 9019. https://dx.doi.org/10.3390/ijms21239019
Le H, Nguyen N H, Ta D T, Le T N T, Bui T P, Le N T, Nguyen C X, Rolletschek H, Stacey G, Stacey M G, Pham N B, Do P T, Chu H H:
CRISPR/Cas9-mediated knockout of galactinol synthase-encoding genes reduces raffinose family oligosaccharide levels in soybean seeds. Front. Plant Sci. 11 (2020) 612942. https://dx.doi.org/10.3389/fpls.2020.612942
Rolletschek H, Schwender J, König C, Chapman K D, Romsdahl T, Lorenz C, Braun H P, Denolf P, van Audenhove K, Munz E, Heinzel N, Ortleb S, Rutten T, McCorkle S, Borysyuk T, Gündel A, Shi H, Vander Auwermeulen M, Bourot S, Borisjuk L:
Cellular plasticity in response to suppression of storage proteins in the Brassica napus embryo. Plant Cell 32 (2020) 2383-2401. https://dx.doi.org/10.1105/tpc.19.00879
Stickel F:
Phänotypische, biochemische und molekulare Untersuchungen von Hordeum vulgare mit modulierter Expression von SWEET-Transportern. (Bachelor Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2020) 90 pp.
Sturtevant D, Lu S, Zhou Z W, Shen Y, Wang S, Song J M, Zhong J, Burks D J, Yang Z Q, Yang Q Y, Cannon A E, Herrfurth C, Feussner I, Borisjuk L, Munz E, Verbeck G F, Wang X, Azad R K, Singleton B, Dyer J M, Chen L L, Chapman K D, Guo L:
The genome of jojoba (Simmondsia chinensis): A taxonomically isolated species that directs wax ester accumulation in its seeds. Sci. Adv. 6 (2020) eaay3240. https://dx.doi.org/10.1126/sciadv.aay3240
Tikhenko N, Alqudah A M, Borisjuk L, Ortleb S, Rutten T, Wu D D, Nagel M, Himmelbach A, Mascher M, Röder M, Ganal M, Sehmisch S, Houben A, Börner A:
DEFECTIVE ENDOSPERM-D1 (Dee-D1) is crucial for endosperm development in hexaploid wheat. Commun. Biol. 3 (2020) 791. https://doi.org/10.1038/s42003-020-01509-9
Druege U, Hilo A, Pérez-Pérez J M, Klopotek Y, Acosta M, Shahinnia F, Zerche S, Franken P, Hajirezaei M R:
Molecular and physiological control of adventitious rooting in cuttings: phytohormone action meets resource allocation. Ann. Bot. 123 (2019) 929–949. https://dx.doi.org/10.1093/aob/mcy234
Gündel A, Rolletschek H, Borisjuk L:
Infrared visualization of sucrose in plants. A novel microspectroscopic method allows sugar mapping across the plant tissue. q-more.chemeurope.com/q-more-articles/279/infrared-visualization-of-sucrose-in-plants.html. (2019)
Gündel A, Rolletschek H, Wagner S, Muszynska A, Borisjuk L:
More insights with infrared. New method enables quantitative visualization of sucrose distribution in plants. Imaging & Microscopy 1 (2019) 28-29.
Gündel A, Rolletschek H, Wagner S, Muszynska A, Borisjuk L:
Mehr sehen mit Infrarot – Quantitative Visualisierung der Saccharose-Verteilung in Pflanzen. GIT Labor-Fachzeitschr. 63 (2019) 38-39.
Gutjahr F T, Munz E, Jakob P M:
Positive chemical exchange contrast in MRI using Refocused Acquisition of Chemical Exchange Transferred Excitations (RACETE). Z. Med. Phys. 29 (2019) 184-191. https://dx.doi.org/10.1016/j.zemedi.2018.05.005
Langer M:
Untersuchungen zur Samenentwicklung bei Cyclamen persicum MILL. – Visualisierung über NMR sowie Lipid- und Phytohormonanalysen. (Master Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2019) 126 pp.
Radchuk V, Sharma R, Potokina E, Radchuk R, Weier D, Munz E, Schreiber M, Mascher M, Stein N, Wicker T, Kilian B, Borisjuk L:
The highly divergent Jekyll genes, required for sexual reproduction, are lineage specific for the related grass tribes Triticeae and Bromeae. Plant J. 98 (2019) 961-974. https://dx.doi.org/10.1111/tpj.14363
Rizzo P, Altschmied L, Stark P, Rutten T, Guendel A, Scharfenberg S, Franke K, Baeumlein H, Wessjohann L, Koch M, Borisjuk L, Sharbel T F:
Discovery of key regulators of dark glands development and hypericin biosynthesis in St. John's wort (Hypericum perforatum). Plant Biotechnol. J. 17 (2019) 2299-2312. https://dx.doi.org/10.1111/pbi.13141
Savchenko T, Rolletschek H, Dehesh K:
Jasmonates-mediated rewiring of central metabolism regulates adaptive responses. Plant Cell Physiol. 60 (2019) 2613-2620. https://dx.doi.org/10.1093/pcp/pcz181
Savchenko T, Rolletschek H, Heinzel N, Tikhonov K, Dehesh K:
Waterlogging tolerance rendered by oxylipin-mediated metabolic reprogramming in Arabidopsis. J. Exp. Bot. 70 (2019) 2919–2932. https://dx.doi.org/10.1093/jxb/erz110
Tedeschi F, Rizzo P, Huong B, Czihal A, Rutten T, Altschmied L, Scharfenberg S, Grosse I, Becker C, Weigel D, Bäumlein H, Kuhlmann M:
EFFECTOR OF TRANSCRIPTION factors are novel plant-specific regulators associated with genomic DNA methylation in Arabidopsis. New Phytol. 221 (2019) 261-278. https://dx.doi.org/10.1111/nph.15439
Wabila C, Neumann K, Kilian B, Radchuk V, Graner A:
A tiered approach to genome-wide association analysis for the adherence of hulls to the caryopsis of barley seeds reveals footprints of selection. BMC Plant Biol. 19 (2019) 95. https://dx.doi.org/10.1186/s12870-019-1694-1
Zornow R:
Untersuchungen zum Keimverhalten von Getreide- und Ölsaaten. (Master Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2019) 99 pp.
Gündel A, Rolletschek H, Wagner S, Muszynska A, Borisjuk L:
Micro imaging displays the sucrose landscape within and along its allocation pathways. Plant Physiol. 178 (2018) 1448-1460. https://dx.doi.org/10.1104/pp.18.00947
Lappe R R, Baier J W, Boehlein S K, Huffman R, Lin Q, Wattebled F, Settles A M, Hannah L C, Borisjuk L, Rolletschek H, Stewart J D, Scott M P, Hennen-Bierwagen T A, Myers A M:
Functions of maize genes encoding pyruvate phosphate dikinase in developing endosperm. Proc. Natl. Acad. Sci. U.S.A. 115 (2018) E24-E33. https://dx.doi.org/10.1073/pnas.1715668115
Lorenz C, Brandt S, Borisjuk L, Rolletschek H, Heinzel N, Tohge T, Fernie A R, Braun H-P, Hildebrandt T M:
The role of persulfide metabolism during Arabidopsis seed development under light and dark conditions. Front. Plant Sci. 9 (2018) 1381. https://dx.doi.org/10.3389/fpls.2018.01381
Meitzel T:
Signaling pathways in legume seed development: evidence for a crosstalk between trehalose 6-phosphate and auxin. (PhD Thesis) Halle/S., Martin-Luther-Universität Halle-Wittenberg, Naturwissenschaftliche Fakultät I Biowissenschaften (2018) 177 pp.
Munz E:
High resolution, physiological and metabolic MRI of plants. (PhD Thesis) Würzburg, Julius-Maximilians-Universität (2018) 170 pp.
Muszynska A:
Histological, ultrastructural, elemental, and molecular genetic characterization of ′Stabilstroh’, a complex trait of rye (Secale cereale L.) determining lodging resistance. (PhD Thesis) Halle/S., Martin-Luther-Universität Halle-Wittenberg, Naturwissenschaftliche Fakultät III Agrar- und Ernährungswissenschaften, Geowissenschaften und Informatik (2018) 161 pp.
Radchuk V, Tran V, Radchuk R, Diaz-Mendoza M, Weier D, Fuchs J, Riewe D, Hensel G, Kumlehn J, Munz E, Heinzel N, Rolletschek H, Martinez M, Borisjuk L:
Vacuolar processing enzyme 4 contributes to maternal control of grain size in barley by executing programmed cell death in the pericarp. New Phytol. 218 (2018) 1127-1142. https://dx.doi.org/10.1111/nph.14729
Rajaraman J, Douchkov D, Lück S, Hensel G, Nowara D, Pogoda M, Rutten T, Meitzel T, Brassac J, Höfle C, Hückelhoven R, Klinkenberg J, Trujillo M, Bauer E, Schmutzer T, Himmelbach A, Mascher M, Lazzari B, Stein N, Kumlehn J, Schweizer P:
Evolutionarily conserved partial gene duplication in the Triticeae tribe of grasses confers pathogen resistance. Genome Biol. 19 (2018) 116. https://dx.doi.org/10.1186/s13059-018-1472-7
Walerowski P, Gündel A, Yahaya N, Truman W, Sobczak M, Olszak M, Rolfe S A, Borisjuk L, Malinowski R:
Clubroot disease stimulates early steps of phloem differentiation and recruits SWEET sucrose transporters within developing galls. Plant Cell 30 (2018) 3058-3073. https://dx.doi.org/10.1105/tpc.18.00283
Borisjuk L:
The inner life of seed: from seeing to understanding. (Habilitation Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2017) 402 pp.
Keil P, Liebsch G, Borisjuk L, Rolletschek H:
MultiSense: a multimodal sensor tool enabling the high throughput analysis of respiration. In: Kapuganti J G (Ed.): Plant respiration and internal oxygen: methods and protocols. (Series: Methods in molecular biology, Vol. 1670) New York, NY [u.a.]: Humana Press (2017) ISBN 978-1-4939-7291-3, 47-56. https://dx.doi.org/10.1007/978-1-4939-7292-0_5
König C:
Molecular and metabolic characterization of assimilate uptake and storage product synthesis in Brassica napus. (PhD Thesis) Hannover, Gottfried Wilhelm Leibniz Universität Hannover, Naturwissenschaftliche Fakultät (2017) 119 pp.
Mascher M, Gundlach H, Himmelbach A, Beier S, Twardziok S O, Wicker T, Radchuk V, Dockter C, Hedley P E, Russell J, Bayer M, Ramsay L, Liu H, Haberer G, Zhang X-Q, Zhang Q, Barrero R A, Li L, Taudien S, Groth M, Felder M, Hastie A, Šimková H, Staňková H, Vrána J, Chan S, Muñoz-Amatriaín M, Ounit R, Wanamaker S, Bolser D, Colmsee C, Schmutzer T, Aliyeva-Schnorr L, Grasso S, Tanskanen J, Chailyan A, Sampath D, Heavens D, Clissold L, Cao S, Chapman B, Dai F, Han Y, Li H, Li X, Lin C, McCooke J K, Tan C, Wang P, Wang S, Yin S, Zhou G, Poland J A, Bellgard M I, Borisjuk L, Houben A, Doležel J, Ayling S, Lonardi S, Kersey P, Langridge P, Muehlbauer G J, Clark M D, Caccamo M, Schulman A H, Mayer K F X, Platzer M, Close T J, Scholz U, Hansson M, Zhang G, Braumann I, Spannagl M, Li C, Waugh R, Stein N:
A chromosome conformation capture ordered sequence of the barley genome. Nature 544 (2017) 427-433. https://dx.doi.org/10.1038/nature22043
McAdam E L, Meitzel T, Quittenden L J, Davidson S E, Dalmais M, Bendahmane A I, Thompson R, Smith J J, Nichols D S, Urquhart S, Gélinas-Marion A, Aubert G, Ross J J:
Evidence that auxin is required for normal seed size and starch synthesis in pea. New Phytol. 216 (2017) 193-204. https://dx.doi.org/10.1111/nph.14690
Munz E, Rolletschek H, Oeltze-Jafra S, Fuchs J, Guendel A, Neuberger T, Ortleb S, Jakob P M, Borisjuk L:
A functional imaging study of germinating oilseed rape seed. New Phytol. 216 (2017) 1181-1190. https://dx.doi.org/10.1111/nph.14736
Radchuk V, Riewe D, Peukert M, Matros A, Strickert M, Radchuk R, Weier D, Steinbiß H-H, Sreenivasulu N, Weschke W, Weber H:
Down-regulated sucrose transporters HvSUT1, HvSUT2 affects sucrose homeostasis along its delivery path in barley grains. J. Exp. Bot. 68 (2017) 4595-4612. https://doi.org/10.1093/jxb/erx266
Reichelt W N, Brillmann M, Thurrold P, Keil P, Fricke J, Herwig C:
Physiological capacities decline during induced bioprocesses leading to substrate accumulation. In: Ferreira G N M, Glassey J (Eds.): Biotechnol. J. (Special Issue: European Symposium on Biochemical Engineering Science, Dublin 2016). (Vol. 7) : WILEY-VCH Verlag (2017) 1860-7314, 1600547. https://dx.doi.org/10.1002/biot.201600547
Rolletschek H, Borisjuk L, Hennen-Bierwagen T A, Myers A M:
Central metabolism and its spatial heterogeneity in maize endosperm. In: Larkins B A (Ed.): Maize kernel development. Boston, MA: CABI (2017) ISBN 978-1-78639-121-6, 134-148.
Rolletschek H, Liebsch G:
A method for imaging oxygen distribution and respiration at a microscopic level of resolution. In: Kapuganti J G (Ed.): Plant respiration and internal oxygen: methods and protocols. (Series: Methods in molecular biology, Vol. 1670) New York, NY [u.a.]: Humana Press (2017) ISBN 978-1-4939-7291-3, 31-38. https://dx.doi.org/10.1007/978-1-4939-7292-0_3
Scherzer S, Shabala L, Hedrich B, Fromm J, Bauer H, Munz E, Jakob P, Al-Rascheid K A S, Kreuzer I, Becker D, Eiblmeier M, Rennenberg H, Shabala S, Bennett M, Neher E, Hedrich R:
Insect haptoelectrical stimulation of Venus flytrap triggers exocytosis in gland cells. Proc. Natl. Acad. Sci. U.S.A. 114 (2017) 4822-4827. https://dx.doi.org/10.1073/pnas.1701860114
Woodfield H K, Sturtevant D, Borisjuk L, Munz E, Guschina I A, Chapman K D, Harwood J L:
Spatial and temporal mapping of key lipid species in Brassica napus seeds. Plant Physiol. 173 (2017) 1998-2009. https://dx.doi.org/10.1104/pp.16.01705
Keller E R J, Grübe M, Hajirezaei M-R, Melzer M, Mock H-P, Rolletschek H, Senula A, Subbarayan K:
Experience in large-scale cryopreservation and links to applied research for safe storage of plant germplasm. In: Lambardi M, Hamill S (Eds.): Proceedings of the XXIX IHC - Int. Symp. on Micropropagation and In Vitro Techniques, Brisbane, Australia, August 17-22, 2014. (Series: Acta Horticulturae, Vol. 1113) Leuven: ISHS (2016) 239-249. https://dx.doi.org/10.17660/ActaHortic.2016.1113.36
Kovalchuk N, Chew W, Sornaraj P, Borisjuk N, Yang N, Singh R, Bazanova N, Shavrukov Y, Guendel A, Munz E, Borisjuk L, Langridge P, Hrmova M, Lopato S:
The homeodomain transcription factor TaHDZipI-2 from wheat regulates frost tolerance, flowering time and spike development in transgenic barley. New Phytol. 211 (2016) 671-687. https://dx.doi.org/10.1111/nph.13919
Munz E, Jakob P M, Borisjuk L:
The potential of nuclear magnetic resonance to track lipids in planta. Biochimie 130 (2016) 97-108. https://dx.doi.org/10.1016/j.biochi.2016.07.014
Datenpublikationen
Psaroudakis D, Neumann K, Rolletschek H, Borisjuk L, Szymanski J:
Time-resolved multi-omics analysis of heat stress response in moneymaker tomato plants. e!DAL - Plant Genomics and Phenomics Research Data Repository (PGP), IPK Gatersleben (2025) https://dx.doi.org/10.5447/IPK/2025/3
Langer M, Hilo A, Guan J-C, Koch K E, Xiao H, Verboven P, Gündel A, Wagner S, Ortleb S, Radchuk V, Mayer S, Nicolai B, Borisjuk L, Rolletschek H:
RNA-seq raw data sets of the developing maize kernel. NCBI GenBank under accession number PRJNA823922 (2023) https://www.ncbi.nlm.nih.gov/bioproject/PRJNA823922
Radchuk V, Szymanski J:
The RNAseq data of the developing barley grains of HvSWEET11b repressed lines vs control. NCBI GenBank under accession number PRJNA852376 (2023) https://www.ncbi.nlm.nih.gov/bioproject/PRJNA852376
scroll top